Mães de todo o país também puderam conversar. Semana de notícias Ansiedade em relação aos seus filhos Depois que a Food and Drug Administration (FDA) rejeitou o tratamento para várias doenças raras e potencialmente fatais.
Uma mãe diz que está “com medo” de perder o acesso a medicamentos como resultado da rejeição pelo FDA de um medicamento do qual sua filha depende. enquanto outras mães também disseram estar preocupadas com quanto tempo conseguiriam ficar com os filhos.
A mãe de um menino de 15 anos com Síndrome de Hunter conta a história. Semana de notícias: “Todas as noites eu o coloco na cama. Me pergunto se será a última vez. Será a última vez que verei meu filho vivo, aquecido e olhando para mim? Ele está sempre lá.”
O porta-voz da FDA disse Semana de notícias: “A FDA está firmemente comprometida em fornecer tratamento e cura às famílias necessitadas da maneira mais segura possível. Isso significa que deve haver evidências claras de benefícios clínicos para a população-alvo de pacientes. As empresas devem demonstrar esse benefício através de dados sólidos de ensaios clínicos bem controlados e conduzidos de forma adequada.”
“Os americanos votaram no FDA que trabalha para eles. Não apenas um apoiador. E a agência está agindo ao se recusar a aprovar o carimbo de borracha. Sob a liderança do comissário Makary, as aprovações do FDA estão no seu nível mais alto. Isso é impulsionado pelo compromisso da agência com a ciência de primeira classe”, acrescentou o porta-voz.
Negação da FDA de tratamento para doenças raras
Segundo a FDA, aproximadamente 30 milhões de americanos vivem com doenças raras. e o próprio comitê da agência disse Considerando o grande número de americanos com doenças raras “Os problemas não são raros. É um apelo à ação”.
O FDA afirma que existem mais de 10.000 doenças raras e aproximadamente metade da população dos EUA. que tiveram uma doença rara quando criança Muitas destas doenças são fatais. E a maioria não recebe tratamentos aprovados. Alguns pacientes com doenças raras têm acesso a potenciais tratamentos através de ensaios clínicos.
A FDA anunciou várias reformas destinadas a acelerar a inovação em doenças raras, incluindo: flexibilidade de bom senso para a produção de células e terapia genética; Implementação de estatísticas bayesianas, que são melhores para pequenas populações de pacientes. Para revisar medicamentos para certas doenças raras Trabalhar com patrocinadores para complementar os dados de ensaios tradicionais com evidências adicionais, como evidências de modelos não clínicos. Dados farmacodinâmicos ou relatório do paciente Entre outras reformas
No entanto, de acordo com Kim Higbee, membro do conselho da Fundação Hope For PDCD, uma organização que defende pessoas com deficiência de piruvato desidrogenase (PDCD), desde o início de janeiro de 2025, a comunidade de doenças raras descobriu que a FDA enviou 23 cartas de resposta completas sobre medicamentos para doenças raras.
A FDA enviará uma carta de resposta completa se decidir que o medicamento não pode ser aprovado na sua forma atual. Isso geralmente significa que o medicamento é rejeitado ou a aprovação é adiada até que uma investigação mais aprofundada sobre segurança e eficácia, uma vez concluído o tratamento.
A rejeição do FDA aos tratamentos para doenças raras gerou muito debate nas últimas semanas. e o senador Ron Johnson disse que, como resultado, iniciaria uma investigação sobre a agência.
Para algumas crianças, a desaprovação de certos tratamentos pelo FDA significa que os medicamentos que estavam tomando em ensaios clínicos podem não estar mais disponíveis. Como resultado, as suas famílias temem o que isso significará para o seu futuro.
PDCD também ganhou atenção recentemente quando o jogador de golfe da PGA Akshay Bhatia disse que depois de vencer o torneio Arnold Palmer International na Flórida no início deste mês, a vitória foi em homenagem a sua neta, que tinha PDCD e morreu em dezembro aos 6 anos.
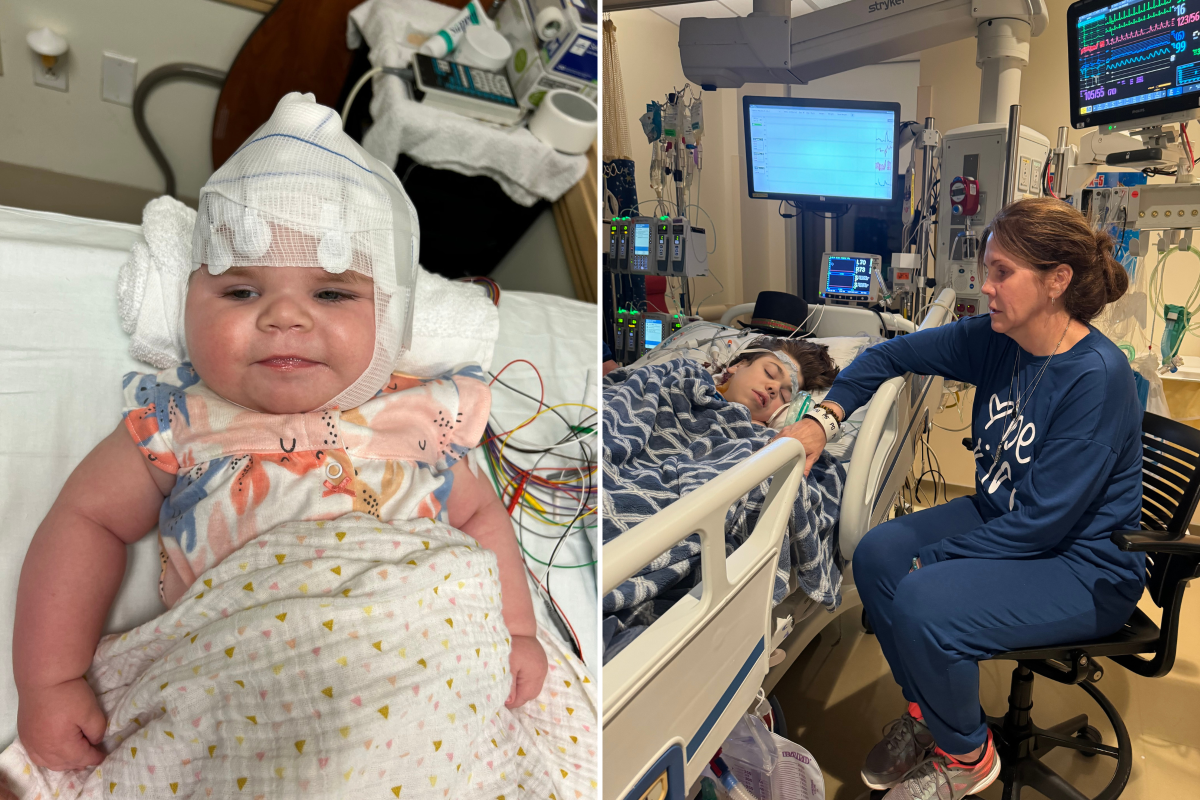
Conheça Cole, um jovem de 15 anos com Síndrome de Hunter.
Uma criança afetada pela falta de aprovação do FDA da terapia genética da síndrome de Hunter RGX-121 da farmacêutica Regenxbio no mês passado é Cole Stephens, de 15 anos.
disse a mãe de Cole, Kim, diretora executiva do Centro de Pesquisa e Tratamento Dr. Joseph Muenzer MPS da Universidade da Carolina do Norte, Chapel Hill. Semana de notícias Ele teve “primeiros dois anos de vida relativamente normais”, mas alguns de seus sintomas exigiram diagnóstico por um especialista em ouvido, nariz e garganta (ENT).
O especialista então alertou Stephens que achava que Cole poderia ter a Síndrome de Hunter “em segundos. Meus sonhos e expectativas familiares para Cole foram destruídos. Meu filho estava morrendo”, disse Stephens. Semana de notícias.
Após seu diagnóstico, haveria uma espera de cerca de dois anos antes que Cole pudesse se submeter a um teste de terapia de reposição enzimática (TRE). Naquela época, Stephens disse que observou Cole de perto em busca de quaisquer mudanças. isso aconteceu com sua condição e deitou-se ao lado dele para que ela pudesse acompanhar sua respiração durante a noite.
Aos 15 anos, Cole não conseguia falar, mas podia passear. Pegue um pouco de comida. e consegue respirar sem ajuda. Ele disse sua última palavra aos 9 anos, que foi “mamãe”.
“Ver seu filho se deteriorar é a coisa mais difícil que você pode imaginar”, disse Stephens. “Depois do diagnóstico, observo todos os dias sinais de progressão da doença. E então começou a acontecer. E eu não consegui impedir. Ele está morrendo e não pude ajudá-lo.”
Na carta de resposta final, a FDA recomendou que a Regenxbio conduzisse um novo estudo. Tratar pacientes adicionais e continuar a acompanhar os resultados do tratamento a longo prazo. Isto atrasará o plano de tratamento quando o medicamento for aprovado.
Há também outro medicamento no radar para a Síndrome de Hunter, o tividenofusp alfa (ou DNL310), mas Stephens disse isso porque esses medicamentos “desistiram e atrasaram. Minha esperança também.”
Stephens disse que espera trabalhar com Johnson na investigação da FDA. “Temos de quebrar o padrão de negação do tratamento para doenças raras e a recusa da FDA em utilizar aprovação acelerada e biomarcadores. A ciência está correcta. E as técnicas estão a matar as nossas crianças”, disse ela.
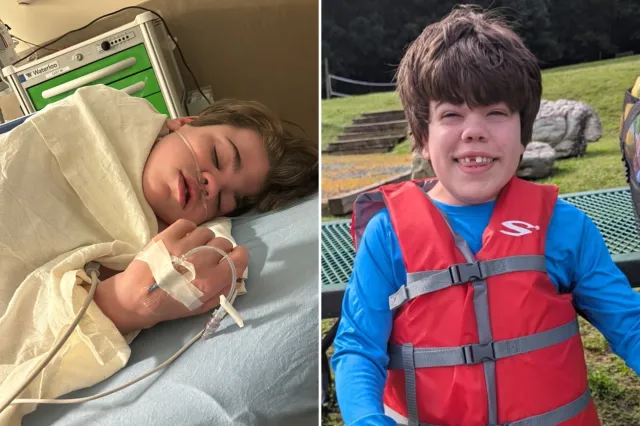
Conheça Harlow, 4, que tem PDCD.
A filha de 4 anos de Kim Higbee, Harlow, tem PDCD, disse Higbee. Semana de notícias desde o nascimento Eles percebem que “havia algo errado” com a saúde de Harlow. e sua jornada até o diagnóstico “Desde o primeiro dia”
Depois que uma ressonância magnética do cérebro deu resultados anormais quando ela tinha 6 meses de idade, as coisas progrediram e os exames revelaram que um lado do cérebro era menor que o outro. Então ela foi rapidamente passada para a genética. Ela acabou sendo diagnosticada com PDCD quando tinha 9 meses de idade.
“Quanto mais você envelhece, mais percebemos que ela não estava progredindo como nosso primeiro filho”, disse Higbee, que tem uma filha de 7 anos, Cassidy.
Quando ela tinha 10 meses, Harlow pôde experimentar. Dicloroacetato (DCA), que é um possível tratamento para PDCD, e Higbee disse que está no “rótulo aberto” do medicamento desde abril de 2023, há quase três anos.
Higbee diz que o tratamento é combinado com uma dieta cetogênica médica. Esta é uma dieta muito rica em gordura e muito pobre em carboidratos. Isso ajudou a condição de Harlow a melhorar significativamente.
“Você pode ver sua janela de vigília se estendendo por mais tempo. Ela ficou mais alerta”, disse Higbee. “Você podia vê-la começando a brincar com os brinquedos. Antes que ela não conseguisse pegar nada e começasse a se sentar.”
Aos 4 anos, Harlow conseguia engatinhar. “Esse foi um grande passo para fazê-la se mover em um movimento de rolamento”, disse Higbee. Harlow também “se levantou com ajuda”, acrescentou sua mãe.
Harlow teve que ser alimentado através de um tubo de alimentação. Portanto, isso pode significar que chegar à escola de manhã é difícil para Higbee, pois ela tem que preparar uma dieta cetogênica para Harlow, alimentá-lo por sonda, o que leva cerca de 30 a 45 minutos, e depois levar suas duas filhas para duas escolas separadas, porque onde Cassidy vai não há apoio específico para crianças com necessidades especiais.
Embora Higbee diga que está “grata pelo quão longe (Harlow) chegou”, há dias em que ela se pergunta. “Por que não é fácil?”
Recentemente, o FDA rejeitou o medicamento PDCD da Saol Therapeutics, um medicamento que Harlow toma há anos. Higbee disse que ela e a comunidade PDCD se sentem “invisíveis porque vemos nossos filhos fazendo coisas que nunca esperávamos que fizessem”.
Ela acrescentou que foi “devastador” e agora a deixou com “medo imediato” sobre se Harlow perderia o medicamento com o qual passou a confiar. Como os fabricantes provavelmente não conseguirão manter o acesso aberto sem a aprovação da FDA, isso destruiu as esperanças de muitas famílias.
“Estamos lutando contra isso o máximo que podemos”, disse Higbee, explicando que viajou várias vezes a Washington, D.C. para falar com legisladores. “Nossa família, que é uma família com uma doença rara. Você não deveria ter que lutar contra o governo enquanto luta pela vida do seu filho.”
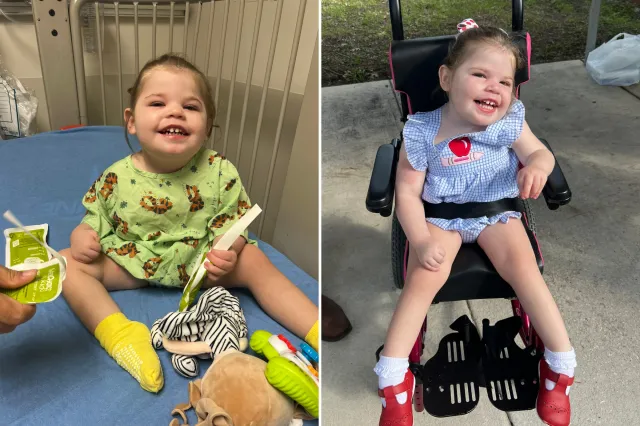
Conheça Violet, uma criança de 4 anos com PDCD.
Outra jovem que vivia com PDCD era a filha de 4 anos de Frances Pimentel, Violet, quando Violet nasceu, disse Pimentel. Semana de notícias Que não havia “sinais de alerta” de que ela não estava saudável. A família recebeu alta hospitalar após o parto. “Estou muito feliz em pensar que nossa família está completa e que a vida continuará normalmente”, disse Pimentel.
Porém, com o passar do tempo, a falta de apetite e a sonolência constante de Violet preocupam Pimentel. Naquela época, ele trabalhava na indústria de alimentação infantil. e ao dar conhecimento ela sentiu algo “seriamente anormal”
Ela tentou obter ajuda médica. Mas ela disse que sentia “há gás venenoso o tempo todo… e me disseram que eu estava exagerando”. Quando Violet tinha 8 meses de idade, suas preocupações foram levadas a sério por uma equipe de genética da Universidade da Califórnia, em São Francisco. Ela acabou sendo diagnosticada com PDCD. Naquela época, Violet não conseguia “olhar para cima, rolar, seguir os brinquedos, ou mesmo segurar um brinquedo”, disse Pimentel.
Assim como Harlow, Violet foi submetida a uma dieta cetogênica médica e alimentada por meio de um tubo de alimentação. e posteriormente inscrita em um ensaio clínico de DCA, “agradecemos a Deus todos os dias por termos tomado essa decisão” de inscrevê-la, disse Pimentel.
Seguindo a trilha por três anos, o progresso de Violet “Foi incrível de ver”, disse Pimentel. Ela foi capaz de expandir um pouco a comida que podia comer. À medida que progride para comer e beber por via oral, caminhe uma curta distância. com ajuda, e “esquecemos quantas palavras ela pode dizer”
Quando Violet foi diagnosticada pela primeira vez, “estou arrasado”, disse Pimentel. Mas sua dor a forçou a agir. E ela fundou a Hope For PDCD, uma organização de defesa dos pacientes liderada pelos pais. “Para mim, canalizar a minha dor para apoiar esta condição tem sido terapêutico para mim”, disse ela, acrescentando. “Ela também estava extremamente orgulhosa de minha filha e de sua determinação.”
Depois que o FDA rejeitou o medicamento que Violet vinha tomando há anos, Pimentel disse que se sentia “assustada e sem esperança” e “com medo de perder o acesso à medicação para Violet e todos os seus irmãos PDCD”.
“No ano passado, as empresas de doenças raras e de biotecnologia enfrentaram cada vez mais recusas e atrasos no FDA, bem como o uso errático e imprevisível das ferramentas regulatórias que o Congresso lhes deu”, disse ela. E para cada criança nascida com PDCD, não podemos permitir que o atraso se torne desastroso.”

Numa era de polarização, o centro foi visto como desrespeitoso. Semana de notíciasO nosso é diferente: o Centro Corajoso não é “ambos os lados”, mas sim perspicaz, desafiador e cheio de ideias. Seguimos fatos, não grupos. Se esse parece ser o tipo de jornalismo que você deseja que tenha sucesso, precisamos de você
Ao se tornar membro da Newsweek, você apoia a missão de manter o centro forte e vibrante. Os membros desfrutam de: Navegação sem anúncios. Conteúdo exclusivo e discussão dos editores Central de Ajuda Seja Corajoso Cadastre-se hoje mesmo